
|
ЕНЦИКЛОПЕДІЯ РАДІОЕЛЕКТРОНІКИ ТА ЕЛЕКТРОТЕХНІКИ Порівняльні характеристики гальванічних елементів типорозміру АА. Енциклопедія радіоелектроніки та електротехніки
Енциклопедія радіоелектроніки та електротехніки / Зарядні пристрої, акумулятори, гальванічні елементи Сьогодні в магазинах та на ринках можна зустріти безліч різних гальванічних елементів. Які вибрати? Пропонована стаття допоможе ухвалити правильне рішення. Для живлення різної радіоелектронної апаратури широко застосовують гальванічні елементи та батареї. Найбільшого поширення набули елементи типорозміру АА. На торгових прилавках можна зустріти подібні вироби різних фірм переважно двох електрохімічних систем: сольові та лужні. Нещодавно фірма Energizer розпочала випуск літієвих гальванічних елементів типорозміру АА напругою 1,5 В. Найважливіша характеристика гальванічного елемента – ємність (кількість електрики, яку він здатний віддати у навантаження) – майже ніколи не вказана на етикетці. Покупцеві залишається орієнтуватися на телевізійні рекламні ролики про елементи, які "працюють до десяти разів довше за звичайні сольові", або повірити на слово фірмі Energizer, яка стверджує, що її нові літієві елементи е2 типорозміру АА працюють у п'ять разів довше за звичайні лужні [1]. Причому залишається цілком зрозумілим, які саме елементи названі " звичайними " . Щоб кількісно порівняти параметри елементів різних електрохімічних систем необхідно випробувати їх в однакових умовах. Такі випробування були проведені з елементами трьох типів: сольовим Philips Long Life (ЕДС "свіжого" елемента - 1,65 В), лужним Duracell Ultra МОЗ (1,62 В) та літієвим Energizer е2 (1,8 В). Кожен був навантажений резистором номіналом 15 Ом, що відповідає початковому струму розрядки приблизно 100 мА. Для елементів типорозміру АА такий струм навантаження типовий. Розрядка проводилася циклами кілька годин на добу, що відповідає реальним умовам експлуатації. Цим пояснюються викиди напруги на розрядних кривих, показаних на рис. 1. Крива синього кольору відповідає сольовому елементу, червоного – лужному та зеленого – літієвому. За час "відпочинку" напруга на елементі будь-якого типу трохи зростала, але після підключення навантаження воно швидко знижувалося до мінімального попереднього циклу. Точками відзначені значення ЕРС елементів – напруги на них без навантаження.
Якщо прийняти як критерій повної розрядки елемента зменшення напруги на його навантаженні до 0,9 В, експериментально певна ємність сольового елемента склала 1 Ач, лужного - 2,9 Ач, а літієвого - 3,5 Ач. Отже, про жодні п'яти- і десятикратні відмінності в ємності елементів різних електрохімічних систем говорити не доводиться. На рис. 2 наведено ще одну серію кривих.
Вони показують, як змінювалося внутрішній опір елементів у процесі розрядки. Відповідність між типом елемента та кольором кривої тут така сама, як на рис. 1. Значення внутрішнього опору R були обчислені за формулою
де Е - ЕРС елемента; U – напруга під навантаженням; RH – опір навантаження. Внутрішній опір сольового та лужного елементів у міру розрядки монотонно зростає. А опір літієвого, різко зменшившись на початку розрядки, до її кінця залишається практично незмінним, та був настільки ж різко збільшується. Звісно, проведені експерименти не можна назвати вичерпними. Місткість елемента не суворо фіксована величина, вона залежить від багатьох зовнішніх факторів. У різних елементів її максимум може досягатися при істотно різних умовах розрядки. Щоб зважити на все це, довелося б провести дуже велику, нереальну в аматорських умовах серію експериментів. Проте спробуємо перевірити одержані результати розрахунком. Щоб оцінити теоретично максимально можливу ємність елементів різних електрохімічних систем, потрібно знати хімічний склад їх електродів, електроліту і хімічну реакцію, що відбувається в елементі. У сольових та лужних елементів катод – цинк, анод – двоокис марганцю. Саме з цієї причини такі елементи узагальнено називають марганцево-цинковими. Але електроліт у них різний: сіль (зазвичай хлорид амонію) або луг (гідроксід калію). За даними [2] у сольовому марганцево-цинковому елементі відбувається реакція
а в лужному
Про матеріал електродів та хімічну реакцію в літієвому елементі немає достовірних відомостей. Можна лише припустити, що електроди – літій та двоокис марганцю, а електроліт – розчин перхлорату літію в пропілен-карбонаті. Якщо цей здогад вірний, згідно [2] в літієвому елементі йде реакція
Використовуючи закон Фарадея, отримаємо вираз визначення ємності гальванічного елемента З, Ач:
де m – маса реагуючих речовин F = 96,5-103 Кл/г-екв – число Фарадея; n - валентність (для сольового та лужного гальванічних елементів - 2, для літієвого - 1); М – сумарна молекулярна маса реагуючих речовин. Зважуємо гальванічні елементи типорозміру АА: сольовий - 17 г, лужний - 24 г, літієвий - 15 г Припустимо, що в порівнянні з масою реагуючих речовин маса корпусу елемента та речовин, що не беруть участі в реакції (вугільний електрод, електроліт у лужному та літієвому елементах) ), мізерно мала і нею можна знехтувати. Сумарну молекулярну масу реагуючих речовин обчислимо з наведених вище рівнянь хімічних реакцій: у сольового – 346 г, у лужного – 257 г, у літієвого – 94 г. Підставляючи у формулу числові значення, отримаємо максимально можливу ємність сольового елемента – 2,6 А-ч , лужного – 5 А-год, літієвого – 4,3 Ач. Відмінності розрахованих значень ємності від виміряних можна пояснити досить грубими припущеннями, прийнятими під час розрахунку. Тож п'яти- та десятикратних відмінностей не виявлено. Теоретична ємність лужного елемента приблизно вдвічі більша за сольову ємність, а літієвий не має в цьому відношенні ніякої переваги перед лужним. Це відповідає результатам експерименту. За підсумками всієї виконаної роботи можна зробити наступне: 1. Літієві гальванічні елементи мають найбільш стабільну напругу, найменший внутрішній опір, який практично не залежить від ступеня розрядженості, і найбільшою, хоча і не набагато, ємністю. Їх краще застосовувати для живлення апаратури з великим споживаним струмом, а також у пристроях, які автоматично відключаються при зниженні напруги джерела живлення (наприклад, цифрові фотоапарати). 2. Лужні елементи мають ємність, порівнянну з ємністю літієвих, також здатні віддавати в навантаження великий струм, проте при меншій напрузі. Їх краще застосовувати у пристроях із середнім струмом споживання без автоматичного контролю напруги. У багатьох випадках лужні елементи краще літієвих, оскільки вони в три-чотири рази дешевші. 3. Сольові елементи мають найменшу ємність та найбільший внутрішній опір. Їх доцільно застосовувати в апаратурі з малим споживаним струмом. література
Автор: І.Подушкін, м.Москва
Машина для проріджування квітів у садах
02.05.2024 Удосконалений мікроскоп інфрачервоного діапазону
02.05.2024 Пастка для комах
01.05.2024
▪ Прилад, керуючий сновидіннями
▪ Розділ сайту Альтернативні джерела енергії. Добірка статей ▪ стаття Біант. Знамениті афоризми ▪ статья Який винахід людини першим подолав звуковий бар'єр? Детальна відповідь ▪ стаття Компасні румби, кутова розмітка. Поради туристу ▪ стаття Простий регулятор потужності на триністорах. Енциклопедія радіоелектроніки та електротехніки
Коментарі до статті: Гість Тлумачна стаття, дякую.
Головна сторінка | Бібліотека | Статті | Карта сайту | Відгуки про сайт www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






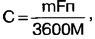
 Залишіть свій коментар до цієї статті:
Залишіть свій коментар до цієї статті: